Um diese Seite in einer anderen Sprache herunterzuladen oder auszudrucken, wählen Sie zunächst Ihre Sprache aus dem Dropdown-Menü oben links aus.

IAOMT-Positionspapier zu Hohlräumen im menschlichen Kieferknochen
Vorsitzender des Ausschusses für Kieferknochenpathologie: Ted Reese, DDS, MAGD, NMD, FIAOMT
Karl Anderson, DDS, MS, NMD, FIAOMT
Patricia Berube, DMD, MS, CFMD, FIAOMT
Jerry Bouquot, DDS, MSD
Teresa Franklin, PhD
Jack Kall, DMD, FAGD, MIAOMT
Cody Kriegel, DDS, NMD, FIAOMT
Sushma Lavu, DDS, FIAOMT
Tiffany Shields, DMD, NMD, FIAOMT
Mark Wisniewski, DDS, FIAOMT
Das Komitee möchte Michael Gossweiler, DDS, MS, NMD, Miguel Stanley, DDS und Stuart Nunally, DDS, MS, FIAOMT, NMD unseren Dank für ihre Kritik an diesem Papier aussprechen. Wir möchten auch die unschätzbaren Beiträge und Bemühungen von Dr. Nunnally bei der Zusammenstellung des Positionspapiers 2014 würdigen. Seine Arbeit, sein Fleiß und seine Praxis bildeten das Rückgrat für dieses aktualisierte Papier.
Genehmigt vom IAOMT-Verwaltungsrat im September 2023
Inhaltsverzeichnis
Kegelstrahl-Computertomographie (CBCT)
Biomarker und histologische Untersuchung
Sich entwickelnde Überlegungen für diagnostische Zwecke
Systemische und klinische Implikationen
Alternative Behandlungsstrategien
Bibliographie
Anhang I Ergebnisse der IAOMT-Umfrage 2
Anhang II Ergebnisse der IAOMT-Umfrage 1
Anhang III Bilder
Abbildung 1 Fettige degenerative Osteonekrose des Kieferknochens (FDOJ)
Abbildung 2 Zytokine in FDOJ im Vergleich zu gesunden Kontrollen
Abbildung 3 Chirurgischer Eingriff bei einem retromolaren FDOJ
Abbildung 4 Kürettage und entsprechendes Röntgenbild des FDOJ
Filme Videoclips von Kieferknochenoperationen bei Patienten
Im letzten Jahrzehnt ist in der Öffentlichkeit und bei Gesundheitsdienstleistern das Bewusstsein für einen Zusammenhang zwischen oraler und systemischer Gesundheit gewachsen. Beispielsweise ist Parodontitis ein Risikofaktor sowohl für Diabetes als auch für Herzerkrankungen. Es wurde auch ein potenziell folgenreicher und zunehmend erforschter Zusammenhang zwischen der Pathologie des Kieferknochens und der allgemeinen Gesundheit und Vitalität des Einzelnen nachgewiesen. Der Einsatz technisch fortschrittlicher Bildgebungsmodalitäten wie der Kegelstrahl-Computertomographie (CBCT) hat maßgeblich zur Identifizierung von Kieferknochenpathologien beigetragen, was zu verbesserten Diagnosemöglichkeiten und einer verbesserten Fähigkeit zur Beurteilung des Erfolgs chirurgischer Eingriffe geführt hat. Wissenschaftliche Berichte, Dokumentationen und soziale Medien haben das öffentliche Bewusstsein für diese Pathologien geschärft, insbesondere bei Personen, die an ungeklärten chronischen neurologischen oder systemischen Erkrankungen leiden, die auf herkömmliche medizinische oder zahnärztliche Eingriffe nicht ansprechen.
Die International Academy of Oral Medicine and Toxicology (IAOMT) basiert auf der Überzeugung, dass die Wissenschaft die Grundlage für die Auswahl und Anwendung aller Diagnose- und Behandlungsmodalitäten sein sollte. Mit dieser Priorität im Hinterkopf stellen wir 1) diese Aktualisierung unseres IAOMT-Positionspapiers zur Jawbone Osteonecrose 2014 vor und 2) schlagen auf der Grundlage histologischer Beobachtungen einen wissenschaftlich und medizinisch genaueren Namen für die Krankheit vor, insbesondere „Chronische ischämische Markkrankheit“. des Kieferknochens (CIMDJ). CIMDJ beschreibt eine Knochenerkrankung, die durch das Absterben zellulärer Bestandteile der Spongiosa infolge einer Unterbrechung der Blutversorgung gekennzeichnet ist. Im Laufe seiner Geschichte wurde das, was wir als CIMDJ bezeichnen, mit einer Vielzahl von Namen und Akronymen bezeichnet, die in Tabelle 1 aufgeführt sind und im Folgenden kurz erläutert werden.
Das Ziel und die Absicht dieser Akademie und des Papiers besteht darin, Patienten und Ärzten Wissenschaft, Forschung und klinische Beobachtungen zur Verfügung zu stellen, damit diese fundierte Entscheidungen bei der Betrachtung dieser CIMDJ-Läsionen treffen können, die oft als Kieferknochenkavitationen bezeichnet werden. Dieses Papier aus dem Jahr 2023 wurde in einer gemeinsamen Anstrengung von Klinikern, Forschern und einem hervorragenden Kieferknochenpathologen, Dr. Jerry Bouquot, nach Durchsicht von über 270 Artikeln erstellt.
In keinem anderen Knochen ist das Risiko für Traumata und Infektionen so groß wie im Kieferknochen. Eine Durchsicht der Literatur zum Thema Kieferknochenkavitation (z. B. CIMDJ) zeigt, dass dieser Zustand seit den 1860er Jahren diagnostiziert, behandelt und erforscht wird. Im Jahr 1867 hielt Dr. HR Noel einen Vortrag mit dem Titel Ein Vortrag über Karies und Knochennekrose am Baltimore College of Dental Surgery und im Jahr 1901 werden Kieferknochenkavitationen ausführlich von William C. Barrett in seinem Lehrbuch mit dem Titel „Oral Pathology and Practice: A Textbook for the Use of Students in Dental Colleges and a Handbook for Dental Practitioners“ erörtert. GV Black, der oft als Vater der modernen Zahnheilkunde bezeichnet wird, fügte in sein Lehrbuch „Special Dental Pathology“ von 1915 einen Abschnitt ein, in dem „das übliche Erscheinungsbild und die Behandlung“ dessen beschrieben wurden, was er als Kieferknochen-Osteonekrose (JON) bezeichnete.
Die Forschung zu Kieferknochenkavitationen schien zum Stillstand zu kommen, bis in den 1970er Jahren andere begannen, sich mit dem Thema zu befassen, verschiedene Namen und Bezeichnungen zu verwenden und Informationen dazu in modernen Lehrbüchern zur oralen Pathologie zu veröffentlichen. Beispielsweise beobachteten Bouquot et al. 1992 eine intraossäre Entzündung bei Patienten mit chronischen und starken Gesichtsschmerzen (N=135) und prägten den Begriff „Neuralgia-inducing Cavitational Osteonecrosis“ oder NICO. Obwohl sich Bouquot et al. nicht zur Ätiologie der Krankheit äußerten, kamen sie zu dem Schluss, dass es wahrscheinlich sei, dass die Läsionen eine chronische Gesichtsneuralgie mit einzigartigen lokalen Merkmalen auslösten: intraossäre Hohlraumbildung und langjährige Knochennekrose mit minimaler Heilung. In einer klinischen Studie mit Patienten mit Trigeminusneuralgie (N=38) und Gesichtsneuralgie (N=33) zeigten Ratner et al. außerdem, dass fast alle Patienten Hohlräume im Alveolarknochen und Kieferknochen aufwiesen. Die Hohlräume mit teilweise mehr als einem Zentimeter Durchmesser befanden sich an den Stellen früherer Zahnextraktionen und waren im Röntgenbild in der Regel nicht erkennbar.

 In der Literatur gibt es eine Vielzahl anderer Begriffe für das, was wir als CIMDJ bezeichnen. Diese sind in Tabelle 1 aufgeführt und werden hier kurz erläutert. Adams et al. prägten 2014 in einem Positionspapier den Begriff „Chronic Fibrosing Osteomyelitis“ (CFO). Das Positionspapier war das Ergebnis eines multidisziplinären Konsortiums von Praktikern aus den Bereichen Oralmedizin, Endodontie, orale Pathologie, Neurologie, Rheumatologie, Hals-Nasen-Ohrenheilkunde, Parodontologie, Psychiatrie, Mund-, Kiefer- und Gesichtsradiologie, Anästhesie, allgemeine Zahnheilkunde, Innere Medizin und Schmerztherapie . Der Schwerpunkt der Gruppe lag auf der Bereitstellung einer interdisziplinären Plattform zur Behandlung von Erkrankungen im Zusammenhang mit Kopf, Hals und Gesicht. Durch die gemeinsamen Bemühungen dieser Gruppe, umfangreiche Literaturrecherchen und Patienteninterviews entstand ein eindeutiges klinisches Muster, das sie als CFO bezeichneten. Sie stellten fest, dass diese Krankheit aufgrund ihrer Komorbidität mit anderen systemischen Erkrankungen häufig nicht diagnostiziert wird. Diese Gruppe wies auf die möglichen Zusammenhänge zwischen der Krankheit und systemischen Gesundheitsproblemen sowie auf die Notwendigkeit eines Ärzteteams hin, um den Patienten ordnungsgemäß zu diagnostizieren und zu behandeln.
In der Literatur gibt es eine Vielzahl anderer Begriffe für das, was wir als CIMDJ bezeichnen. Diese sind in Tabelle 1 aufgeführt und werden hier kurz erläutert. Adams et al. prägten 2014 in einem Positionspapier den Begriff „Chronic Fibrosing Osteomyelitis“ (CFO). Das Positionspapier war das Ergebnis eines multidisziplinären Konsortiums von Praktikern aus den Bereichen Oralmedizin, Endodontie, orale Pathologie, Neurologie, Rheumatologie, Hals-Nasen-Ohrenheilkunde, Parodontologie, Psychiatrie, Mund-, Kiefer- und Gesichtsradiologie, Anästhesie, allgemeine Zahnheilkunde, Innere Medizin und Schmerztherapie . Der Schwerpunkt der Gruppe lag auf der Bereitstellung einer interdisziplinären Plattform zur Behandlung von Erkrankungen im Zusammenhang mit Kopf, Hals und Gesicht. Durch die gemeinsamen Bemühungen dieser Gruppe, umfangreiche Literaturrecherchen und Patienteninterviews entstand ein eindeutiges klinisches Muster, das sie als CFO bezeichneten. Sie stellten fest, dass diese Krankheit aufgrund ihrer Komorbidität mit anderen systemischen Erkrankungen häufig nicht diagnostiziert wird. Diese Gruppe wies auf die möglichen Zusammenhänge zwischen der Krankheit und systemischen Gesundheitsproblemen sowie auf die Notwendigkeit eines Ärzteteams hin, um den Patienten ordnungsgemäß zu diagnostizieren und zu behandeln.
Kavitationsläsionen im Kieferknochen wurden auch bei Kindern beobachtet. Im Jahr 2013 beschrieben Obel et al. Läsionen bei Kindern und prägten den Begriff Juvenile Mandibular Chronic Osteomyelitis (JMCO). Diese Gruppe schlug den möglichen Einsatz intravenöser (IV) Bisphosphonate zur Behandlung dieser Kinder vor. Im Jahr 2016 veröffentlichten Padwa et al. eine Studie, in der eine fokale sterile entzündliche Osteitis im Kieferknochen von pädiatrischen Patienten beschrieben wurde. Sie bezeichneten die Läsion als pädiatrische chronische nichtbakterielle Osteomyelitis (CNO).
Seit 2010 erforschen Dr. Johann Lechner, der meistveröffentlichte Autor und Forscher zu Kavitationsläsionen des Kieferknochens, und andere den Zusammenhang dieser Läsionen mit der Zytokinproduktion, insbesondere dem entzündlichen Zytokin RANTES (auch bekannt als CCL5). Dr. Lechner hat verschiedene Begriffe verwendet, um diese Läsionen zu beschreiben, darunter die zuvor erwähnte NICO, aber auch die aseptische ischämische Osteonekrose im Kieferknochen (AIOJ) und die fettige degenerative Osteonekrose im Kieferknochen (FDOJ). Seine Beschreibung/Bezeichnung basiert auf dem körperlichen Erscheinungsbild und/oder dem makroskopisch pathologischen Zustand, der klinisch oder intraoperativ beobachtet wird.
Es besteht nun Bedarf an der Klärung einer weiteren, kürzlich identifizierten Kieferknochenpathose, die sich vom Thema dieser Arbeit unterscheidet, für diejenigen, die Kavitationsläsionen erforschen, jedoch verwirrend sein könnte. Hierbei handelt es sich um knöcherne Verletzungen des Kiefers, die durch die Einnahme von Arzneimitteln entstehen. Die Läsionen sind am besten durch einen Verlust der Blutversorgung mit anschließender unkontrollierbarer Knochensequestrierung gekennzeichnet. Diese Läsionen wurden von Ruggiero et al. in einem Positionspapier für Oral Ulceration with Bone Sequestration (OUBS) genannt Amerikanische Vereinigung der Mund- und Kieferchirurgen (AAOMS) sowie von Palla et al. in einer systematischen Übersicht. Da dieses Problem mit der Verwendung eines oder mehrerer Arzneimittel zusammenhängt, ist das IAOMT der Meinung, dass diese Art von Läsion am besten als medikamentenbedingte Osteonekrose des Kiefers (MRONJ) beschrieben werden kann. MRONJ wird in diesem Artikel nicht besprochen, da sich seine Ätiologie und Behandlungsansätze von denen der sogenannten CIMDJ unterscheiden und es bereits ausführlich untersucht wurde.
Die immer häufigere Verwendung von Röntgenaufnahmen mit Kegelstrahl-Computertomographie (CBCT) durch viele Zahnärzte hat dazu geführt, dass die intramedullären Kavitationen, die wir als CIMDJ bezeichnen, häufiger beobachtet werden und die zuvor übersehen und daher ignoriert wurden. Da diese Läsionen und Anomalien nun leichter zu erkennen sind, liegt es in der Verantwortung der Zahnärzte, die Krankheit zu diagnostizieren und Behandlungsempfehlungen und Pflege zu geben.
Die Anerkennung und Identifizierung der Existenz von CIMDJ ist der Ausgangspunkt für sein Verständnis. Ungeachtet der vielen Namen und Akronyme, die mit der Pathologie in Verbindung gebracht werden, ist das Vorhandensein von nekrotischem oder absterbendem Knochen im medullären Teil des Kieferknochens gut belegt.
Bei der Beobachtung während einer Operation zeigen sich diese Knochendefekte auf vielfältige Weise. Einige Ärzte berichten, dass über 75 % der Läsionen vollständig hohl oder mit weichem, graubraunem und demineralisiertem/granulomatisiertem Gewebe gefüllt sind, oft mit gelbem öligem Material (Ölzysten) in den defekten Bereichen mit umgebender normaler Knochenanatomie. Andere berichten über das Vorhandensein von Kavitationen mit unterschiedlicher Dichte der darüber liegenden kortikalen Knochen, die beim Öffnen eine Auskleidung mit faserigen schwarzen, braunen oder grauen filamentösen Materialien zu haben scheinen. Wieder andere berichten von groben Veränderungen, die verschiedentlich als „kiesig“, „wie Sägemehl“, „hohle Hohlräume“ und „trocken“ mit gelegentlicher sklerotischer, zahnartiger Härte der Hohlraumwände beschrieben werden. Bei der histologischen Untersuchung ähneln diese Läsionen der Nekrose, die in anderen Knochen des Körpers auftritt, und unterscheiden sich histologisch von einer Osteomyelitis (siehe Abbildung 1). Weitere Bilder zur Veranschaulichung der CIMDJ-Krankheit, einige davon sind grafischer Natur, sind in Anhang III am Ende dieses Dokuments enthalten.
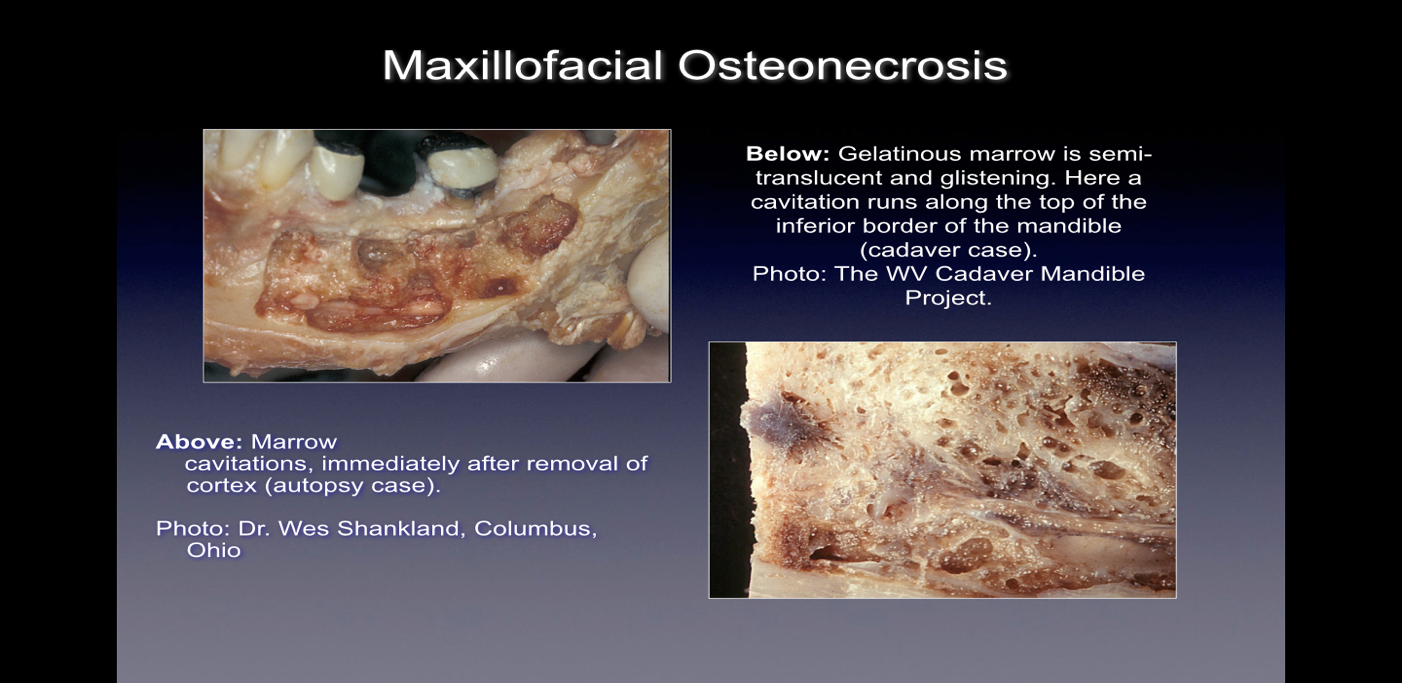
Figure 1 Bilder von CIMDJ, aufgenommen von einer Leiche
Wie andere medizinische Fachkräfte nutzen Zahnärzte einen organisierten Prozess, der verschiedene Methoden und Modalitäten zur Diagnose von Kavitationsläsionen nutzt. Diese können aus der Durchführung einer körperlichen Untersuchung bestehen, die die Erhebung einer Krankengeschichte, die Beurteilung der Symptome, die Entnahme von Körperflüssigkeiten zur Durchführung von Labortests und die Entnahme von Gewebeproben für Biopsien und mikrobiologische Tests (d. h. Tests auf das Vorhandensein von Krankheitserregern) umfasst. Auch bildgebende Verfahren wie die DVT kommen häufig zum Einsatz. Bei Patienten mit komplexen Störungen, die nicht immer einem Muster folgen oder in die typische Reihenfolge eines Symptomkomplexes passen, kann der Diagnoseprozess eine detailliertere Analyse erfordern, die zunächst möglicherweise nur zu einer Differenzialdiagnose führt. Nachfolgend finden Sie kurze Beschreibungen einiger dieser Diagnosemodalitäten.
Kegelstrahl-Computertomographie (CBCT)
Diagnosetechniken, die bereits 1979 von Ratner und Kollegen beschrieben wurden und die digitale Palpation und Druck, diagnostische Lokalanästhetika-Injektionen, die Berücksichtigung der Krankengeschichte und der Lokalisierung ausstrahlender Schmerzen nutzen, sind bei der Diagnose von Kieferknochenkavitationen nützlich. Während einige dieser Läsionen jedoch Schmerzen, Schwellungen, Rötungen und sogar Fieber verursachen, ist dies bei anderen nicht der Fall. Daher ist häufig eine objektivere Maßnahme, beispielsweise eine Bildgebung, erforderlich.
Auf standardmäßigen zweidimensionalen (2D-, z. B. periapikalen und Panorama-)Röntgenfilmen, die üblicherweise in der Zahnheilkunde verwendet werden, werden Kavitationen normalerweise nicht erkannt. Ratner und Kollegen haben gezeigt, dass 40 % oder mehr des Knochens verändert werden müssen, um Veränderungen zu zeigen. Dies wird durch spätere Arbeiten gestützt und in Abbildung 2 dargestellt. Dies hängt mit der inhärenten Einschränkung der 2D-Bildgebung zusammen, die zu Überlagerungen führt von anatomischen Strukturen, Maskierung von Interessenbereichen. Bei Defekten oder Pathologien, insbesondere im Unterkiefer, kann die maskierende Wirkung des dichten kortikalen Knochens auf die darunter liegenden Strukturen erheblich sein. Daher sind technologisch fortschrittliche bildgebende Verfahren wie CBCT, Tech 99-Scans, Magnetresonanztomographie (MRT) oder transalveoläre Ultraschallsonographie (CaviTAU™®) erforderlich.
Von den verschiedenen verfügbaren bildgebenden Verfahren ist das CBCT das am häufigsten verwendete Diagnoseinstrument, das von Zahnärzten bei der Diagnose oder Behandlung von Kavitationen eingesetzt wird, und daher wird es auch ausführlich besprochen. Der Eckpfeiler der CBCT-Technologie ist ihre Fähigkeit, eine interessierende Läsion in drei Dimensionen (frontal, sagittal, koronal) zu betrachten. Die CBCT hat sich als zuverlässige und genaue Methode zur Identifizierung und Schätzung der Größe und des Ausmaßes intraossärer Defekte im Kiefer erwiesen, mit weniger Verzerrungen und geringerer Vergrößerung als 3D-Röntgenaufnahmen.
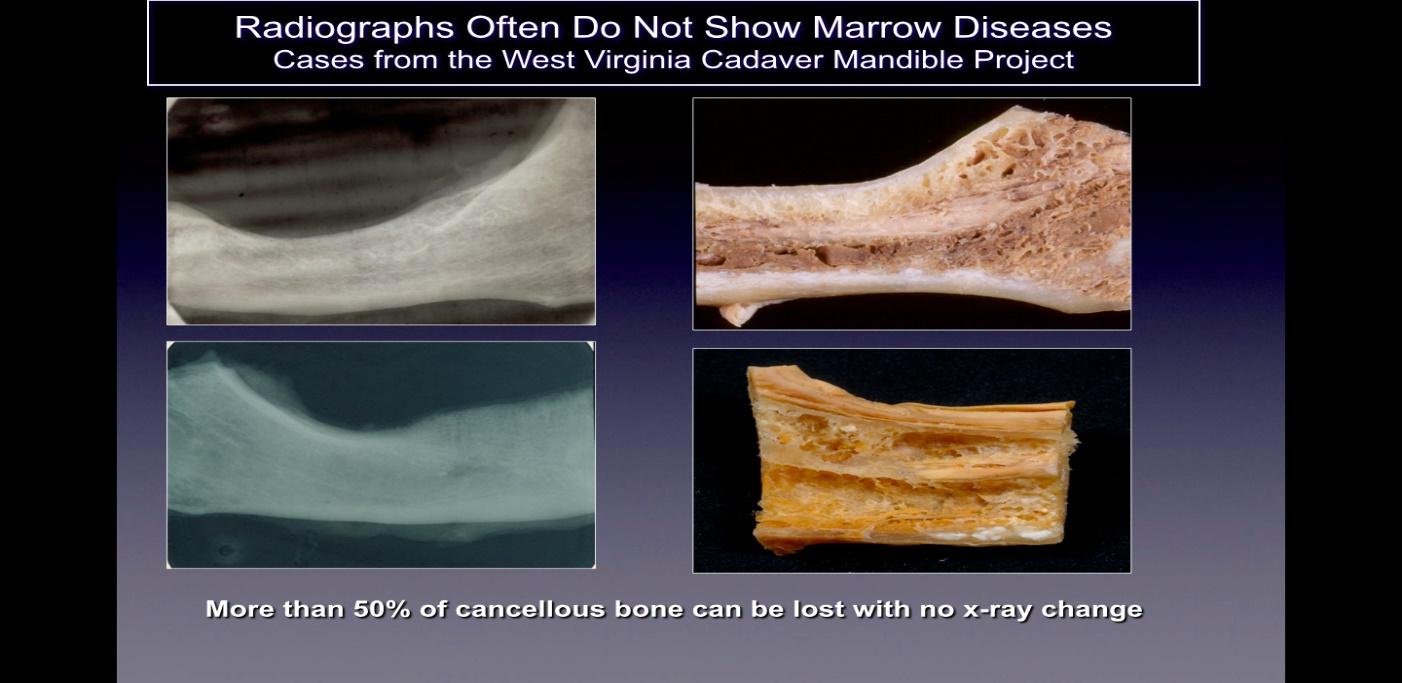
Figure 2 Bildunterschrift: Auf der linken Seite sind 2D-Röntgenaufnahmen von Kieferknochen von aufgetauchten Leichen zu sehen
gesund. Auf der rechten Seite der Abbildung sind Fotos derselben Kieferknochen zu sehen, die offensichtlich nekrotische Kavitation zeigen.
Abbildung nach Bouquot, 2014.
Klinische Studien haben gezeigt, dass DVT-Bilder auch bei der Bestimmung des Inhalts einer Läsion (flüssigkeitsgefüllt, granulomatös, fest usw.) hilfreich sind und möglicherweise dabei helfen, zwischen entzündlichen Läsionen, odontogenen oder nicht odontogenen Tumoren, Zysten und anderen gutartigen oder bösartigen Erkrankungen zu unterscheiden Läsionen.
Kürzlich entwickelte Software, die speziell in verschiedene Arten von DVT-Geräten integriert ist, nutzt Hounsfield-Einheiten (HU), was eine standardisierte Beurteilung der Knochendichte ermöglicht. HU stellen die relative Dichte von Körpergewebe gemäß einer kalibrierten Graustufenskala dar, die auf Werten für Luft (-1000 HU), Wasser (0 HU) und Knochendichte (+1000 HU) basiert. Abbildung 3 zeigt verschiedene Ansichten eines modernen DVT-Bildes.
Zusammenfassend lässt sich sagen, dass sich die CBCT bei der Diagnose und Behandlung von Kieferknochenkavitationen als nützlich erwiesen hat:
- Identifizieren der Größe, Ausdehnung und 3D-Position einer Läsion;
- Identifizieren der Nähe einer Läsion zu anderen nahegelegenen lebenswichtigen anatomischen Strukturen wie z
Nervus alveolaris inferior, Kieferhöhle oder angrenzende Zahnwurzeln;
- Festlegung des Behandlungsansatzes: Operation versus nicht-chirurgisch; Und
- Bereitstellung eines Folgebildes zur Feststellung des Heilungsgrades und der möglichen Notwendigkeit
eine Läsion erneut behandeln.
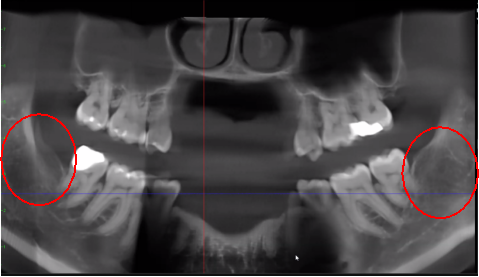
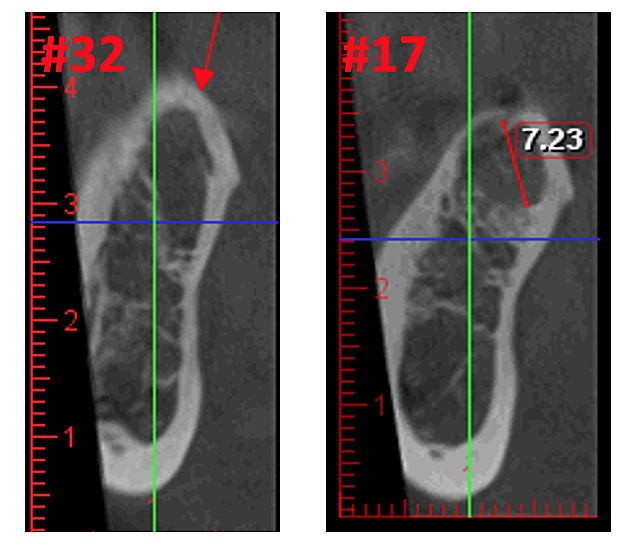
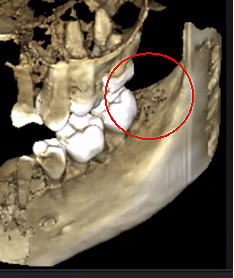
Figure 3 Verbesserte Klarheit des DVT-Bildes durch verfeinerte Softwaretechnologie, die Artefakte und „Rauschen“ reduziert, die Zahnimplantate und Metallrestaurationen im Bild verursachen können. Dadurch können Zahnarzt und Patient die Läsion besser erkennen. Das obere Bild ist eine Panoramaansicht eines DVT, die links (#17) und rechts (#32) die Lage und das Ausmaß der Kavitationsläsionen bei einem Kieferknochen-Osteonekrose-Patienten zeigt. Das untere linke Feld ist eine Sagittalansicht jeder Stelle. Das untere rechte Feld ist eine 3D-Darstellung von Standort Nr. 17, die kortikale Porosität über Markkavitation zeigt. Mit freundlicher Genehmigung von Dr. Reese.
Wir erwähnen hier auch kurz ein Ultraschallgerät, das CaviTAU™®, das entwickelt wurde und in Teilen Europas eingesetzt wird, insbesondere zur Erkennung von Bereichen mit geringer Knochendichte im Ober- und Unterkieferknochen, die auf Kieferknochenkavitationen hinweisen. Dieses transalveoläre Ultraschall-Sonographiegerät (TAU-n) ist im Vergleich zur DVT bei der Erkennung von Kieferknochenmarksdefekten möglicherweise gleichwertig und hat den zusätzlichen Vorteil, dass der Patient einer viel geringeren Strahlenbelastung ausgesetzt ist. Dieses Gerät ist derzeit in den USA nicht erhältlich, wird jedoch von der US-amerikanischen Food and Drug Administration geprüft und könnte sehr wohl das wichtigste Diagnoseinstrument sein, das in Nordamerika zur Behandlung von CIMJD eingesetzt wird.
Biomarker und histologische Untersuchung
Aufgrund der entzündlichen Natur von Kieferknochenkavitationen haben Lechner und Baehr 2017 den möglichen Zusammenhang zwischen ausgewählten Zytokinen und der Krankheit untersucht. Ein Zytokin von besonderem Interesse ist „bei Aktivierung reguliert, normale T-Zellen exprimiert und sezerniert“ (RANTES). Dieses Zytokin sowie der Fibroblasten-Wachstumsfaktor (FGF)-2 werden in Kavitationsläsionen und bei Patienten mit CIMDJ in größeren Mengen exprimiert. Abbildung 4, bereitgestellt von Dr. Lechner, vergleicht die RANTES-Werte bei Patienten mit Kavitation (roter Balken, links) mit den Werten bei gesunden Kontrollpersonen (blauer Balken) und zeigt Werte, die bei Patienten mit dieser Erkrankung mehr als 25-mal höher sind. Lechner et al. verwenden zwei Ansätze zur Messung der Zytokinspiegel. Eine besteht darin, die Zytokinspiegel systemisch im Blut zu messen (Diagnostic Solutions Laboratory, USA.). Eine zweite Methode besteht darin, eine Biopsie direkt an der erkrankten Stelle zu entnehmen, wenn diese zur Beurteilung durch einen Oralpathologen zugänglich ist. Leider erfordert die lokalisierte Gewebeentnahme derzeit eine komplexe Verarbeitung und einen komplexen Versand, der in Nicht-Forschungseinrichtungen noch nicht möglich ist, aber aufschlussreiche Zusammenhänge liefert.
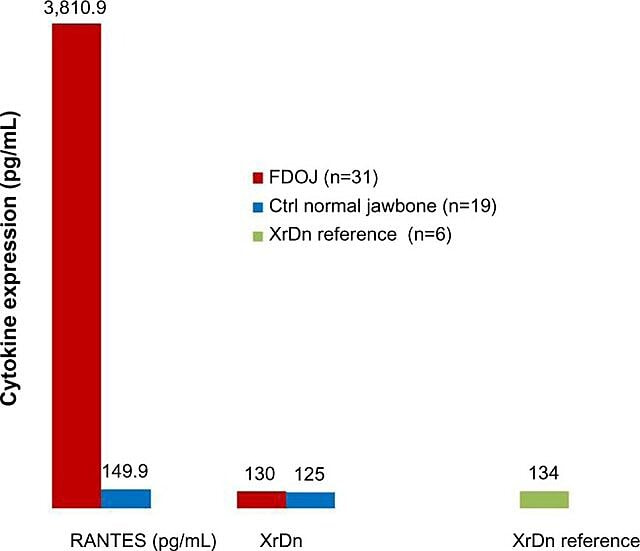
Figure 4 Verteilung von RANTES in 31 FDOJ-Fällen und 19 Proben normaler Kieferknochen im Vergleich zu einer Röntgendichtereferenz für beide Gruppen in den entsprechenden Bereichen. Abkürzungen: RANTES, reguliert bei Aktivierung, normale T-Zellen exprimieren und sezernieren Chemokin (CC-Motiv) Ligand 5; XrDn, Röntgendichte; FDOJ, fettige degenerative Osteonekrose des Kieferknochens; n, Zahl; Strg, Kontrolle. Abbildung bereitgestellt von Dr. Lechner. Amtliches Kennzeichen: CC BY-NC 3.0
Sich entwickelnde Überlegungen für diagnostische Zwecke
Das Vorhandensein von Kieferknochenkavitationen ist klinisch gut belegt. Allerdings müssen eindeutige Diagnosen und bewährte Behandlungsparameter noch weiter erforscht werden. Vor diesem Hintergrund ist es notwendig, kurz einige faszinierende und potenziell wertvolle Techniken zu erwähnen, die von einigen Praktikern verwendet werden.
Es ist anerkannt, dass zusätzliche physiologische Untersuchungen ein wertvolles Screening- und Diagnoseinstrument darstellen würden. Ein solches Werkzeug, das von einigen Praktikern verwendet wird, ist die Thermografie. Eine generalisierte Entzündungsaktivität kann durch die Messung von Wärmeunterschieden auf der Oberfläche von Kopf und Hals beobachtet werden. Die Thermographie ist sicher, schnell und kann einen ähnlichen diagnostischen Wert haben wie die DVT. Ein wesentlicher Nachteil besteht darin, dass es an Definition mangelt, was es schwierig macht, den Rand oder das Ausmaß einer Läsion zu erkennen.
Einige Ärzte untersuchen das energetische Profil einer Läsion mithilfe der Akupunktur-Meridian-Bewertung (AMA), um deren Wirkung auf den entsprechenden Energiemeridian zu bestimmen. Diese Art der Beurteilung basiert auf der Elektroakupunktur nach Voll (EAV). Diese Technik, die auf den Prinzipien der alten chinesischen Medizin und Akupunktur basiert, wurde in den USA entwickelt und wird dort gelehrt. Akupunktur wird eingesetzt, um Schmerzen zu lindern und die Heilung zu fördern. Es basiert auf dem Gleichgewicht des Energieflusses (z. B. Chi) durch bestimmte Energiebahnen im Körper. Diese Bahnen oder Meridiane verbinden bestimmte Organe, Gewebe, Muskeln und Knochen miteinander. Akupunktur nutzt ganz bestimmte Punkte auf einem Meridian, um die Gesundheit und Vitalität aller Körperelemente auf diesem Meridian zu beeinflussen. Diese Technik wurde verwendet, um Kieferknochenerkrankungen aufzudecken, die, wenn sie behoben werden, auch scheinbar nicht zusammenhängende Krankheiten wie Arthritis oder chronisches Müdigkeitssyndrom behandeln können. Diese Technik eignet sich für weitere Untersuchungen (dh die Ergebnisse müssen dokumentiert und Längsschnittdaten erfasst und verbreitet werden).
Es gibt viele einzelne Faktoren, die das Risiko für die Entwicklung von Kieferknochenkavitationen erhöhen, aber in der Regel ist das Risiko multifaktoriell. Risiken für den Einzelnen können sowohl äußere Einflüsse wie Umweltfaktoren als auch innere Einflüsse wie eine schlechte Immunfunktion sein. In den Tabellen 2 und 3 sind externe und interne Risikofaktoren aufgeführt.


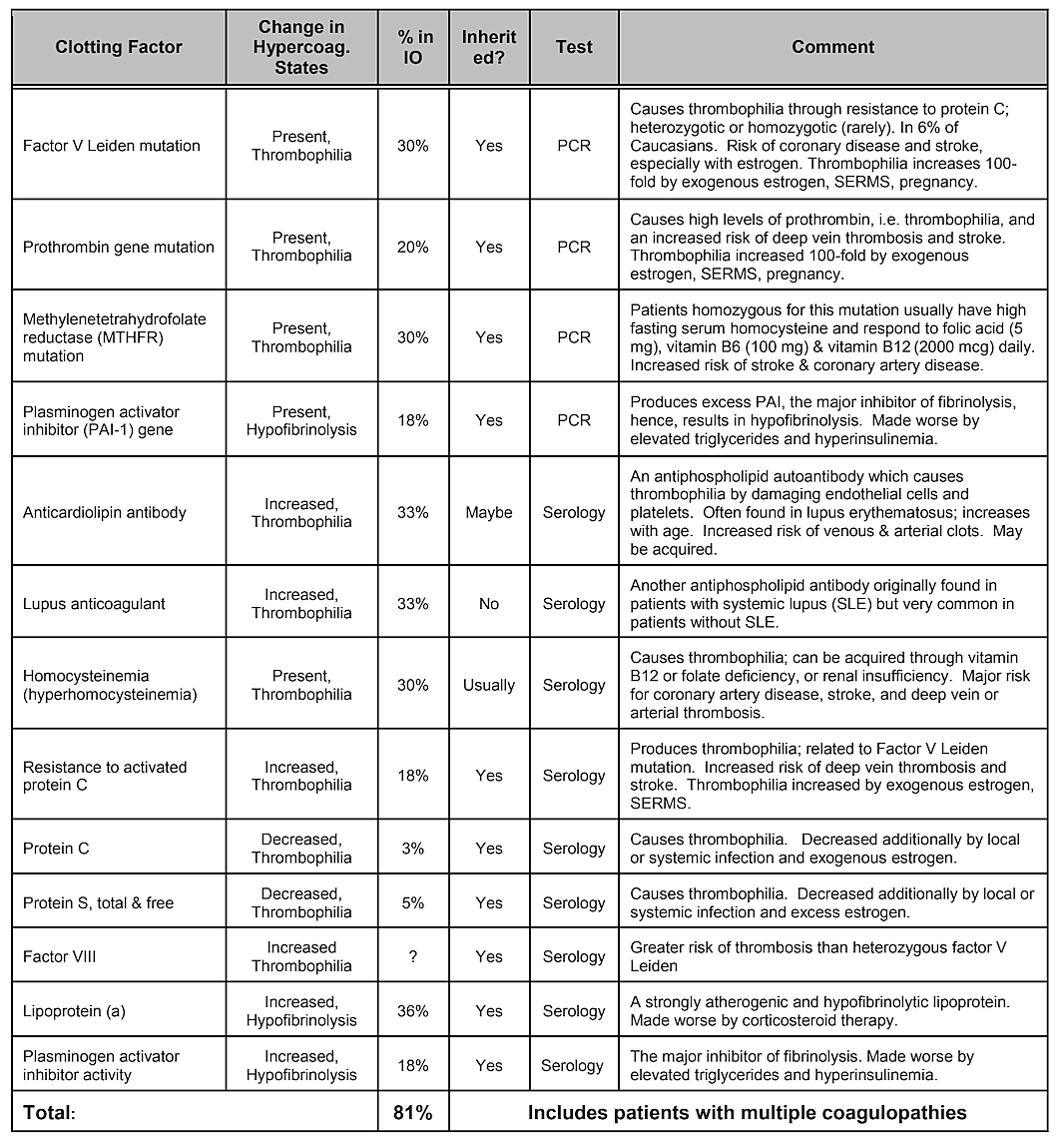
Beachten Sie, dass Tabelle 2, Interne Risikofaktoren, keine genetische Veranlagung enthält. Man geht zwar davon aus, dass genetische Varianzen eine Rolle spielen, Es konnte nicht nachgewiesen werden, dass eine einzelne Genvariation oder gar eine Kombination von Genen ein Risikofaktor ist, genetische Einflüsse sind jedoch wahrscheinlich . Eine im Jahr 2019 durchgeführte systematische Literaturrecherche ergab, dass eine Reihe von Einzelnukleotidpolymorphismen identifiziert wurden, es jedoch keine Replikation zwischen den Studien gibt. Die Autoren kamen zu dem Schluss, dass angesichts der Vielfalt der Gene, die positive Assoziationen mit Kavitationen gezeigt haben, und der mangelnden Reproduzierbarkeit der Studien die Rolle genetischer Ursachen moderat und heterogen zu sein scheint. Es kann jedoch erforderlich sein, bestimmte Bevölkerungsgruppen gezielt anzusprechen, um genetische Unterschiede zu identifizieren. Tatsächlich ist, wie gezeigt wurde, einer der häufigsten und grundlegendsten pathophysiologischen Mechanismen ischämischer Knochenschäden eine übermäßige Gerinnung aufgrund von Hyperkoagulationszuständen, die normalerweise genetische Grundlagen haben, wie von Bouquot und Lamarche (1999) beschrieben. Tabelle 4 von Dr. Bouquot listet die Krankheitszustände auf, die eine Hyperkoagulation beinhalten, und die nächsten drei Absätze bieten einen Überblick über einige der Erkenntnisse von Dr. Bouquot, die er in seiner Rolle als Forschungsdirektor am Maxillofacial Center for Education and Research präsentierte.
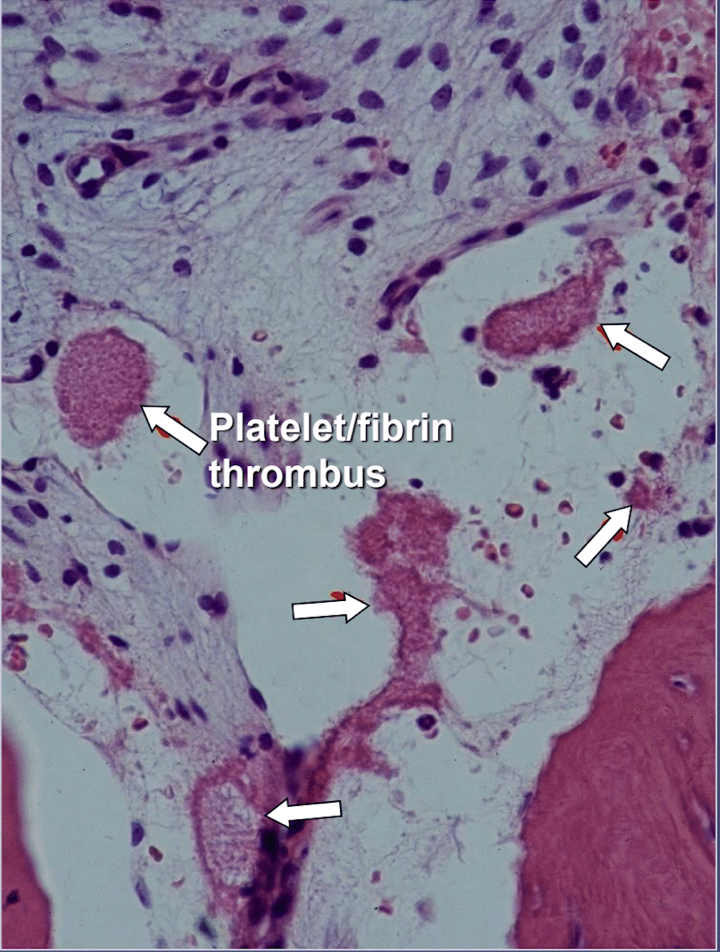
Bei Kieferknochenkavitationen gibt es eindeutige Hinweise auf eine ischämische Osteonekrose, eine Knochenmarkserkrankung, bei der der Knochen aufgrund von Sauerstoff- und Nährstoffmangel nekrotisch wird. Wie bereits erwähnt, können viele Faktoren zusammenwirken und Kavitationen hervorrufen, und bis zu 80 % der Patienten leiden unter einem meist erblich bedingten Problem der übermäßigen Bildung von Blutgerinnseln in ihren Blutgefäßen. Bei routinemäßigen Blutuntersuchungen wird diese Krankheit normalerweise nicht festgestellt. Knochen sind besonders anfällig für dieses Problem der Hyperkoagulation und entwickeln stark erweiterte Blutgefäße; erhöhter, oft schmerzhafter innerer Druck; Blutstau; und sogar Infarkte. Dieses Hyperkoagulationsproblem könnte durch eine familiäre Vorgeschichte von Schlaganfällen und Herzinfarkten in einem frühen Alter (unter 55 Jahren), einem Hüftgelenkersatz oder „Arthritis“ (insbesondere in einem frühen Alter) oder einer Osteonekrose (insbesondere in einem frühen Alter) nahegelegt werden Venenthrombose, Lungenembolie (Blutgerinnsel in der Lunge), Netzhautvenenthrombose (Blutgerinnsel in der Netzhaut des Auges) und wiederkehrende Fehlgeburten. Der Kiefer hat bei dieser Krankheit zwei spezifische Probleme: 2) Ist der erkrankte Knochen einmal geschädigt, ist er kaum noch in der Lage, leichten Infektionen durch Zahn- und Zahnfleischbakterien standzuhalten; und 1) der Knochen erholt sich möglicherweise nicht von der verminderten Durchblutung, die durch die von Zahnärzten bei zahnärztlichen Arbeiten verwendeten Lokalanästhetika verursacht wird. Abbildung 2 zeigt eine mikroskopische Ansicht eines intravaskulären Thrombus.
Tabelle 4 Krankheitszustände, die eine Hyperkoagulation beinhalten. Vier von fünf Patienten mit Kieferknochenkavitation leiden an einer dieser Gerinnsel
Faktorprobleme.
Unabhängig von der zugrunde liegenden Ursache der Hyperkoagulation entwickelt der Knochen entweder ein faseriges Knochenmark (Fasern können in nährstoffarmen Bereichen leben), ein fettiges, totes Fettknochenmark („Nassfäule“) oder ein sehr trockenes, manchmal ledriges Knochenmark („Hausfäule“). ) oder ein völlig hohler Markraum („Kavitation“).
Jeder Knochen kann betroffen sein, am häufigsten sind jedoch Hüfte, Knie und Kiefer betroffen. Die Schmerzen sind oft stark, aber etwa 1/3rd der Patienten verspüren keine Schmerzen. Der Körper hat Schwierigkeiten, sich von dieser Krankheit zu heilen und 2/3rds In den meisten Fällen ist die chirurgische Entfernung des geschädigten Knochenmarks erforderlich, üblicherweise durch Abkratzen mit Küretten. Eine Operation wird das Problem (und die Schmerzen) in fast drei Vierteln beseitigenths der Patienten mit Kieferbeteiligung, obwohl bei 40 % der Patienten wiederholte Operationen, in der Regel kleinere Eingriffe als beim ersten, erforderlich sind, manchmal auch in anderen Teilen des Kiefers, da die Krankheit so häufig „Skip“-Läsionen (d. h. mehrere Stellen im Kiefer) aufweist gleiche oder ähnliche Knochen), mit normalem Knochenmark dazwischen. Mehr als die Hälfte der Hüftpatienten erkranken letztendlich an der gegenüberliegenden Hüfte. Mehr als 1/3rd der Kieferknochenpatienten erkranken an anderen Kieferquadranten. Kürzlich wurde festgestellt, dass 40 % der Patienten mit Osteonekrose der Hüfte oder des Kiefers auf eine Antikoagulation mit Heparin mit niedrigem Molekulargewicht (Lovenox) oder Coumadin mit einer Schmerzlinderung und einer Knochenheilung ansprechen.
Figure 5 Mikroskopische Ansicht intravaskulärer Thromben
Wenn Sie einen nicht-pharmazeutischen Ansatz zur Reduzierung des Risikos einer Hyperkoagulation suchen, können Sie die Verwendung zusätzlicher Enzyme wie Nattokinase oder der stärkeren Lumbrokinase in Betracht ziehen, die beide fibrinolytische und gerinnungshemmende Eigenschaften haben. Darüber hinaus sollten Kupfermangelzustände, die mit Gerinnungsstörungen einhergehen, aufgrund des bei Patienten mit Kieferknochenkavitation beobachteten erhöhten Risikos einer Hyperkoagulation ausgeschlossen werden.
SYSTEMISCHE UND KLINISCHE AUSWIRKUNGEN
Das Vorhandensein von Kieferknochenkavitationen und die damit verbundene Pathologie umfassen einige spezifische Symptome, umfassen jedoch häufig auch einige unspezifische systemische Symptome. Daher sollte das Pflegeteam die Diagnose und Behandlung sorgfältig abwägen. Die einzigartigsten und bahnbrechendsten Erkenntnisse, die seit dem IAOMT-Positionspapier 2014 ans Licht gekommen sind, sind die Lösung scheinbar unabhängiger chronischer Entzündungszustände nach einer Kavitationsbehandlung. Unabhängig davon, ob systemische Erkrankungen autoimmuner Natur sind oder anderweitig auftretende Entzündungen auftreten, wurden signifikante Verbesserungen berichtet, einschließlich einer Verbesserung bei Krebs. Der mit diesen Läsionen verbundene Symptomkomplex ist stark individualisiert und daher nicht verallgemeinerbar oder leicht erkennbar. Daher ist das IAOMT der Ansicht, dass, wenn bei einem Patienten Kieferknochenkavitationen mit oder ohne damit verbundene lokale Schmerzen diagnostiziert werden und außerdem andere systemische Erkrankungen vorliegen, die bisher nicht auf Kieferknochenkavitationen zurückzuführen waren, der Patient einer weiteren Untersuchung bedarf, um festzustellen, ob die Krankheit damit zusammenhängt oder eine Folge der Krankheit ist. Das IAOMT hat seine Mitglieder befragt, um mehr darüber zu erfahren, welche systemischen Symptome/Erkrankungen nach einer Kavitationsoperation verschwinden. Die Ergebnisse sind in Anhang I dargestellt.
Das Vorhandensein von Zytokinen, die in schlecht vaskularisierten, nekrotischen Läsionen von Kieferknochenkavitationen erzeugt werden, scheint als Fokus entzündlicher Zytokine zu fungieren, die andere Entzündungsbereiche aktiv und/oder chronisch halten. Die Linderung oder zumindest Besserung lokalisierter Kieferschmerzen nach der Behandlung wird erhofft und erwartet, aber diese fokale Theorie der Entzündung, die weiter unten ausführlich besprochen wird, könnte erklären, warum so viele scheinbar „nicht zusammenhängende“ Krankheiten mit chronischen Entzündungszuständen in Zusammenhang stehen werden auch durch die Kavitationsbehandlung verringert.
Zur Untermauerung der im Positionspapier des IAOMT aus dem Jahr 2014 gezogenen Schlussfolgerungen zum Zusammenhang zwischen Kieferknochenkavitationen und systemischen Erkrankungen zeigen Forschungsarbeiten und klinische Studien, die kürzlich von Lechner, von Baehr und anderen veröffentlicht wurden, dass Kieferknochenkavitationsläsionen ein spezifisches Zytokinprofil enthalten, das bei anderen Knochenpathologien nicht zu finden ist . Im Vergleich zu gesunden Kieferknochenproben zeigen Kavitationspathologien kontinuierlich eine starke Hochregulierung des Fibroblasten-Wachstumsfaktors (FGF-2), des Interleukin-1-Rezeptorantagonisten (Il-1ra) und, was besonders wichtig ist, von RANTES. RANTES, auch bekannt als CCL5 (cc Motiv Ligand 5), wurde als chemotaktisches Zytokin mit starker proinflammatorischer Wirkung beschrieben. Es wurde gezeigt, dass diese Chemokine in mehreren Phasen der Immunantwort eingreifen und maßgeblich an verschiedenen pathologischen Zuständen und Infektionen beteiligt sind. Studien haben gezeigt, dass RANTES an vielen systemischen Erkrankungen wie Arthritis, chronischem Müdigkeitssyndrom, atopischer Dermatitis, Nephritis, Kolitis, Alopezie, Schilddrüsenerkrankungen und der Förderung von Multipler Sklerose und Parkinson-Krankheit beteiligt ist. Darüber hinaus wurde gezeigt, dass RANTES das Tumorwachstum beschleunigt.
Fibroblasten-Wachstumsfaktoren wurden auch mit Kieferknochenkavitationen in Verbindung gebracht. Die Fibroblasten-Wachstumsfaktoren FGF-2 und die damit verbundenen Rezeptoren sind für viele entscheidende Funktionen verantwortlich, darunter Zellproliferation, Überleben und Migration. Sie sind außerdem anfällig dafür, von Krebszellen gekapert zu werden und spielen bei vielen Krebsarten eine onkogene Rolle. Beispielsweise fördert FGF-2 das Fortschreiten von Tumoren und Krebs bei Prostatakrebs. Darüber hinaus haben die FGF-2-Spiegel einen direkten Zusammenhang mit dem Fortschreiten, der Metastasierung und der schlechten Überlebensprognose bei Patienten mit Darmkrebs gezeigt. Im Vergleich zu krebsfreien Kontrollpersonen weisen Patienten mit Magenkarzinom deutlich höhere FGF-2-Spiegel im Serum auf. Diese Entzündungsbotenstoffe sind an vielen schweren Krankheiten beteiligt, sei es entzündlicher Natur oder krebsartiger Natur. Im Gegensatz zu RANTES/CCL5 und FGF-2 wirkt IL1-ra nachweislich als starker entzündungshemmender Mediator und trägt dazu bei, dass bei einigen Kavitationsläsionen keine häufigen Entzündungszeichen auftreten.
Die übermäßigen RANTES- und FGF-2-Spiegel in Kavitationsläsionen wurden verglichen und mit den bei anderen systemischen Erkrankungen wie Amyotropher Lateralsklerose (ALS), Multipler Sklerose (MS), rheumatoider Arthritis und Brustkrebs beobachteten Spiegeln in Verbindung gebracht. Tatsächlich sind die in Kieferknochenkavitationen nachgewiesenen Konzentrationen dieser Botenstoffe höher als im Serum und in der Gehirn-Rückenmarks-Flüssigkeit von ALS- und MS-Patienten. Aktuelle Forschungen von Lechner und von Baehr haben einen 26-fachen Anstieg von RANTES in osteonekrotischen Läsionen des Kieferknochens von Brustkrebspatientinnen gezeigt. Lechner und Kollegen schlagen vor, dass durch Kavitation gewonnenes RANTES die Entwicklung und das Fortschreiten von Brustkrebs beschleunigen könnte.
Wie bereits erwähnt, gibt es zahlreiche Fälle asymptomatischer Kieferknochenkavitationen. In diesen Fällen werden akute proinflammatorische Zytokine wie TNF-alpha und IL-6 NICHT in erhöhter Zahl in den pathohistologischen Befunden von Kavitationsproben beobachtet. Bei diesen Patienten ist das Fehlen dieser proinflammatorischen Zytokine mit hohen Konzentrationen eines entzündungshemmenden Zytokin-Interleukin-1-Rezeptor-Antagonisten (Il-1ra) verbunden. Die vernünftige Schlussfolgerung ist, dass akute Entzündungen, die mit Kieferknochenkavitationen einhergehen, unter der Kontrolle hoher RANTES/FGF-2-Spiegel stehen. Um eine Diagnose zu stellen, schlagen Lechner und von Baehr daher vor, den Schwerpunkt nicht mehr auf das Vorhandensein einer Entzündung zu legen, sondern den Signalweg zu berücksichtigen, vor allem über die Überexpression von RANTES/FGF-2. Die hohen RANTES/FGF-2-Spiegel bei Kavitationspatienten weisen darauf hin, dass diese Läsionen ähnliche und sich gegenseitig verstärkende pathogene Signalwege zu anderen Organen verursachen könnten. Das Immunsystem wird als Reaktion auf Gefahrensignale aktiviert, die verschiedene angeborene molekulare Wege hervorrufen, die in der Produktion entzündlicher Zytokine und möglicherweise der Aktivierung des adaptiven Immunsystems gipfeln. Dies stützt die Idee und Theorie, dass Kieferknochenkavitationen über die RANTES/FGF-2-Produktion eine grundlegende Ursache für chronische Entzündungserkrankungen sein können, und erklärt außerdem, warum akute Entzündungssymptome in den Kieferknochenläsionen vom Patienten nicht immer gesehen oder gespürt werden sich. Daher stellen Kieferknochenkavitationen und diese beteiligten Botenstoffe einen integrativen Aspekt entzündlicher Erkrankungen dar und dienen als mögliche Ätiologie der Erkrankung. Die Beseitigung von Kavitationen kann ein Schlüssel zur Heilung entzündlicher Erkrankungen sein. Dies wird durch die Beobachtung einer Verringerung der Serum-RANTES-Spiegel nach dem chirurgischen Eingriff bei 5 Brustkrebspatientinnen gestützt (siehe Tabelle 5). Weitere Untersuchungen und Tests der RANTES/CCL5-Werte könnten Aufschluss über diesen Zusammenhang geben. Die ermutigenden Beobachtungen sind die Verbesserungen der Lebensqualität, die viele Patienten mit Kieferhöhlenkavitation verzeichnen, sei es eine Linderung an der Operationsstelle oder eine Linderung chronischer Entzündungen oder Krankheiten an anderer Stelle.
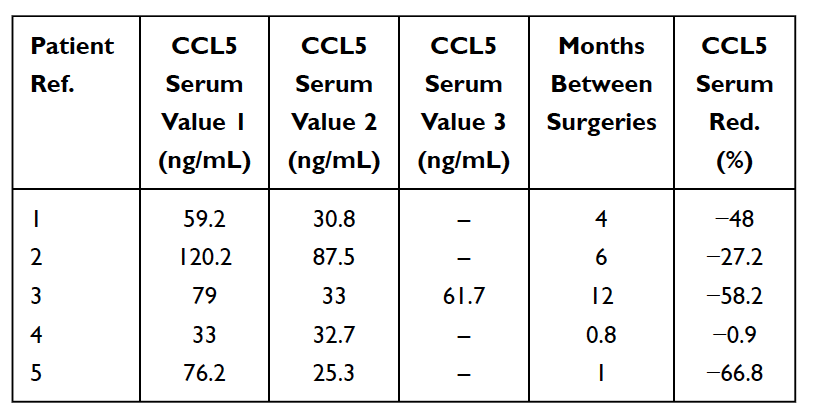
Tabelle 5
Reduzierung (Red.) von RANTES/CCL5 im Serum bei 5 Brustkrebspatientinnen, die sich einer Operation wegen fettig-degenerativer Osteonekrose des Kieferknochens (FDOJ) unterzogen hatten. Tabelle angepasst von
Lechner et al., 2021. Kavitation im Kieferknochen ausgedrückt RANTES/CCL5: Fallstudien, die eine stille Entzündung im Kieferknochen mit der Epistemologie von Brustkrebs verbinden.“ Brustkrebs: Ziele und Therapie.
Aufgrund des Mangels an Literatur zur Behandlung von Kavitationsläsionen befragte das IAOMT seine Mitglieder, um Informationen darüber zu sammeln, welche Trends und Behandlungen sich in Richtung eines „Pflegestandards“ entwickeln. Die Ergebnisse der Umfrage werden in Anhang II kurz besprochen.
Sobald Ort und Größe der Läsionen bestimmt sind, sind Behandlungsmodalitäten erforderlich. Das IAOMT ist der Ansicht, dass es generell inakzeptabel ist, „tote Knochen“ im menschlichen Körper zu belassen. Dies basiert auf Daten, die darauf hindeuten, dass Kieferknochenkavitationen der Ausgangspunkt für systemische Zytokine und Endotoxine sein können, die den Prozess der Verschlechterung der allgemeinen Gesundheit eines Patienten einleiten können.
Unter idealen Umständen sollte eine Biopsie durchgeführt werden, um die Diagnose einer Kieferknochenpathologie zu bestätigen und andere Krankheitszustände auszuschließen. Dann ist eine Behandlung erforderlich, um die betroffene Pathologie zu beseitigen oder zu beseitigen und das Nachwachsen normaler, lebenswichtiger Knochen zu stimulieren. Derzeit scheint in der von Experten begutachteten Literatur die chirurgische Therapie, die aus der Entfernung des betroffenen nicht lebenswichtigen Knochens besteht, die bevorzugte Behandlung für Kieferknochenkavitationen zu sein. Die Behandlung beinhaltet die Verwendung von Lokalanästhetika, was zu einem wichtigen Gesichtspunkt führt. Bisher wurde davon ausgegangen, dass epinephrinhaltige Anästhetika mit bekannten vasokonstriktorischen Eigenschaften bei Patienten vermieden werden sollten, bei denen möglicherweise bereits eine krankheitsbedingte Durchblutungsstörung vorliegt. In einer Reihe molekularer Studien wurde jedoch festgestellt, dass die Differenzierung der Osteoblasten mit der Anwendung von Adrenalin zunahm. Daher muss der Arzt von Fall zu Fall entscheiden, ob Adrenalin verwendet werden soll und, wenn ja, welche Menge verwendet werden sollte, um die besten Ergebnisse zu erzielen.
Nach einer chirurgischen Dekortikation und gründlichen Kürettage der Läsion und Spülung mit steriler normaler Kochsalzlösung wird die Heilung durch die Platzierung von Transplantaten aus plättchenreichem Fibrin (PRF) in den Knochenhohlraum gefördert. Der Einsatz von plättchenreichen Fibrinkonzentraten bei chirurgischen Eingriffen ist nicht nur unter Gerinnungsgesichtspunkten vorteilhaft, sondern auch unter dem Aspekt der Freisetzung von Wachstumsfaktoren über einen Zeitraum von bis zu vierzehn Tagen nach der Operation. Vor der Verwendung von PRF-Transplantaten und anderen Zusatztherapien kam es in bis zu 40 % der Fälle zu einem Rückfall der osteonekrotischen Läsion des Kieferknochens nach der Operation.
Eine Durchsicht der in Tabelle 2 aufgeführten externen Risikofaktoren legt nahe, dass ungünstige Ergebnisse durch geeignete Operationstechnik und Interaktion zwischen Arzt und Patient vermieden werden können, insbesondere in anfälligen Bevölkerungsgruppen. Es ist ratsam, den Einsatz atraumatischer Techniken in Betracht zu ziehen, parodontale und andere Zahnerkrankungen zu minimieren oder zu verhindern und ein Instrumentarium zu wählen, das die besten Heilungsergebnisse ermöglicht. Die Bereitstellung gründlicher prä- und postoperativer Anweisungen für den Patienten, einschließlich der Risiken im Zusammenhang mit dem Rauchen von Zigaretten, kann dazu beitragen, negative Folgen zu minimieren.
Unter Berücksichtigung der breiten Liste potenzieller Risikofaktoren, die in den Tabellen 2 und 3 aufgeführt sind, wird eine Konsultation mit dem erweiterten Pflegeteam des Patienten empfohlen, um mögliche versteckte Risikofaktoren, die zur Entwicklung von Kieferknochenkavitationen beitragen können, ordnungsgemäß zu ermitteln. Eine wichtige Überlegung bei der Behandlung von Kieferknochenkavitationen ist beispielsweise, ob die Person Antidepressiva, insbesondere selektive Serotonin-Wiederaufnahmehemmer (SSRIs), einnimmt. SSRIs wurden mit einer verringerten Knochendichte und erhöhten Frakturraten in Verbindung gebracht. Der SSRI Fluoxetin (Prozac) hemmt direkt die Differenzierung und Mineralisierung von Osteoblasten. Mindestens zwei unabhängige Studien, in denen SSRI-Benutzer im Vergleich zu Kontrollpersonen untersucht wurden, haben gezeigt, dass die Verwendung von SRRI mit schlechteren panoramamorphometrischen Indizes verbunden ist.
Auch eine Vorkonditionierung kann zu erfolgreichen Behandlungsergebnissen beitragen. Dazu gehört die Schaffung einer Gewebeumgebung, die der Heilung förderlich ist, indem der Körper mit ausreichenden Mengen geeigneter Nährstoffe versorgt wird, die das biologische Terrain verbessern, indem sie die Homöostase im Körper optimieren. Vorkonditionierungstaktiken sind nicht immer möglich oder für den Patienten akzeptabel, sie sind jedoch wichtiger für Patienten mit bekannten Anfälligkeiten, beispielsweise solchen mit genetischer Veranlagung, Heilungsstörungen oder beeinträchtigter Gesundheit. In solchen Fällen ist es von entscheidender Bedeutung, dass diese Optimierung erfolgt, um das Ausmaß des oxidativen Stresses zu minimieren, der nicht nur den Krankheitsprozess stimulieren, sondern auch die gewünschte Heilung beeinträchtigen kann.
Idealerweise sollte die Reduzierung jeglicher toxischer Belastung des Körpers wie Fluorid und/oder Quecksilber durch Zahnamalgamfüllungen vor der Behandlung von Kieferknochenkavitationen abgeschlossen sein. Quecksilber kann Eisen in der Elektronentransportkette der Mitochondrien verdrängen. Dies führt zu einem Überschuss an freiem Eisen (Eisen oder Fe++), wodurch schädliche reaktive Sauerstoffspezies (ROS) entstehen, die auch als freie Radikale bekannt sind und oxidativen Stress verursachen. Überschüssiges Eisen im Knochengewebe hemmt auch die ordnungsgemäße Funktion der Osteoblasten, was sich offensichtlich negativ auf die Heilung einer Knochenerkrankung auswirkt.
Auch andere Mängel sollten vor der Behandlung behoben werden. Bei einem Mangel an bioverfügbarem Kupfer, Magnesium und Retinol kommt es zu Störungen des Stoffwechsels und der Wiederverwertung von Eisen im Körper, was zu einem Überschuss an freiem Eisen an den falschen Stellen führt, was zu noch größerem oxidativem Stress und dem Krankheitsrisiko führt. Genauer gesagt werden viele Enzyme im Körper (z. B. Coeruloplasmin) inaktiv, wenn nicht genügend bioverfügbares Kupfer, Magnesium und Retinol vorhanden sind, was dann zu einer systemischen Eisendysregulation und dem daraus resultierenden Anstieg von oxidativem Stress und Krankheitsrisiko führt.
Alternative Behandlungsstrategien
Alternative Techniken, die als primäre oder unterstützende Therapie eingesetzt werden, sollten ebenfalls evaluiert werden. Dazu gehören Homöopathie, elektrische Stimulation, Lichttherapie wie Photobiomodulation und Laser, medizinischer Sauerstoff/Ozon, hyperbarer Sauerstoff, Antikoagulationsmodalitäten, Sanum-Heilmittel, Ernährung und Nutrazeutika, Infrarotsauna, intravenöse Ozontherapie, Energiebehandlungen und andere. Zum jetzigen Zeitpunkt liegen keine wissenschaftlichen Untersuchungen vor, die bestätigen würden, dass diese alternativen Behandlungsformen entweder durchführbar oder unwirksam sind. Es sollten Pflegestandards festgelegt werden, um eine ordnungsgemäße Heilung und Entgiftung sicherzustellen. Techniken zur Erfolgsbewertung sollten getestet und standardisiert werden. Zur Beurteilung sollten Protokolle oder Verfahren vorgelegt werden, die dabei helfen, festzustellen, wann eine Behandlung angemessen ist und wann nicht.
Untersuchungen haben gezeigt, dass das Vorhandensein von Kavitationen im Kieferknochen ein heimtückischer Krankheitsprozess ist, der mit einer verminderten Durchblutung einhergeht. Eine beeinträchtigte Markdurchblutung führt zu einer schlecht mineralisierten und unzureichenden Vaskularisierung in Bereichen des Kieferknochens, die mit Krankheitserregern infiziert werden können, was den Zelltod begünstigt. Der träge Blutfluss in Kavitationsläsionen erschwert die Zufuhr von Antibiotika, Nährstoffen und Immunbotenstoffen. Die ischämische Umgebung kann auch chronische Entzündungsmediatoren beherbergen und fördern, die möglicherweise noch schädlichere Auswirkungen auf die systemische Gesundheit haben. Genetische Veranlagung, verminderte Immunfunktion, die Wirkung bestimmter Medikamente, Traumata und Infektionen sowie andere Faktoren wie Rauchen können die Entwicklung von Kieferknochenkavitationen auslösen oder beschleunigen.
Zusammen mit dem renommierten Kieferknochenpathologen Dr. Jerry Bouquot präsentiert und fördert das IAOMT eine histologisch und pathologisch korrekte Identifizierung von kavitationsbedingten Kieferknochenläsionen als chronische ischämische medulläre Erkrankung des Kieferknochens (CIMDJ). Obwohl in der Vergangenheit und auch heute noch viele Namen, Akronyme und Begriffe zur Bezeichnung dieser Krankheit verwendet werden, ist das IAOMT davon überzeugt, dass dies der am besten geeignete Begriff ist, um den pathologischen und mikrohistologischen Zustand zu beschreiben, der häufig bei Kieferknochenkavitationen auftritt.
Obwohl die meisten Kavitationsläsionen des Kieferknochens mit routinemäßigen Röntgenaufnahmen schwer zu diagnostizieren sind und die meisten nicht schmerzhaft sind, sollte man niemals davon ausgehen, dass der Krankheitsprozess nicht existiert. Es gibt viele Krankheitsprozesse, die schwer zu diagnostizieren sind, und viele, die nicht schmerzhaft sind. Wenn wir Schmerzen als Indikator für die Behandlung verwenden würden, würden Parodontitis, Diabetes und die meisten Krebsarten unbehandelt bleiben. Heutzutage verfügt der Zahnarzt über ein breites Spektrum an Methoden zur erfolgreichen Behandlung von Kieferhöhlenkavitationen. Das Versäumnis, die Krankheit zu erkennen und eine Behandlung zu empfehlen, ist nicht weniger schwerwiegend als das Versäumnis, eine parodontale Erkrankung zu diagnostizieren und zu behandeln. Für die Gesundheit und das Wohlbefinden unserer Patienten ist ein Paradigmenwechsel für alle Angehörigen der Gesundheitsberufe, einschließlich Zahnärzte und Ärzte, von entscheidender Bedeutung, um 1) die Prävalenz von Kieferknochenkavitationen zu erkennen und 2) den Zusammenhang zwischen Kieferknochenkavitationen und systemischen Erkrankungen anzuerkennen.
ERGEBNISSE DER IAOMT-UMFRAGE 2 (2023)
Wie in der Arbeit kurz erörtert, verschwinden nicht verwandte Erkrankungen häufig nach einer Kavitationsoperation. Um mehr darüber zu erfahren, welche Arten von Erkrankungen sich bessern und wie es im Zusammenhang mit der Operation zu einer proximalen Remission kommt, wurde eine zweite Umfrage an die IAOMT-Mitglieder verschickt. Für die Umfrage wurde eine Liste der Symptome und Zustände zusammengestellt, bei denen Mitglieder dieses Ausschusses eine Besserung nach der Operation beobachtet haben. Die Befragten wurden gefragt, ob sie beobachtet hatten, dass einer dieser Zustände nach der Operation zurückging, und wenn ja, in welchem Ausmaß. Sie wurden auch gefragt, ob die Symptome schnell nachließen oder ob die Besserung länger als zwei Monate anhielt. Darüber hinaus wurden die Befragten gefragt, ob sie typischerweise Operationen an einzelnen Stellen, an mehreren einseitigen Stellen oder an allen Stellen in einem Eingriff durchführten. Die Ergebnisse der Umfrage sind in den folgenden Abbildungen dargestellt. Die Daten sind vorläufig, da die Zahl der Befragten gering war (33) und einige Daten fehlen.
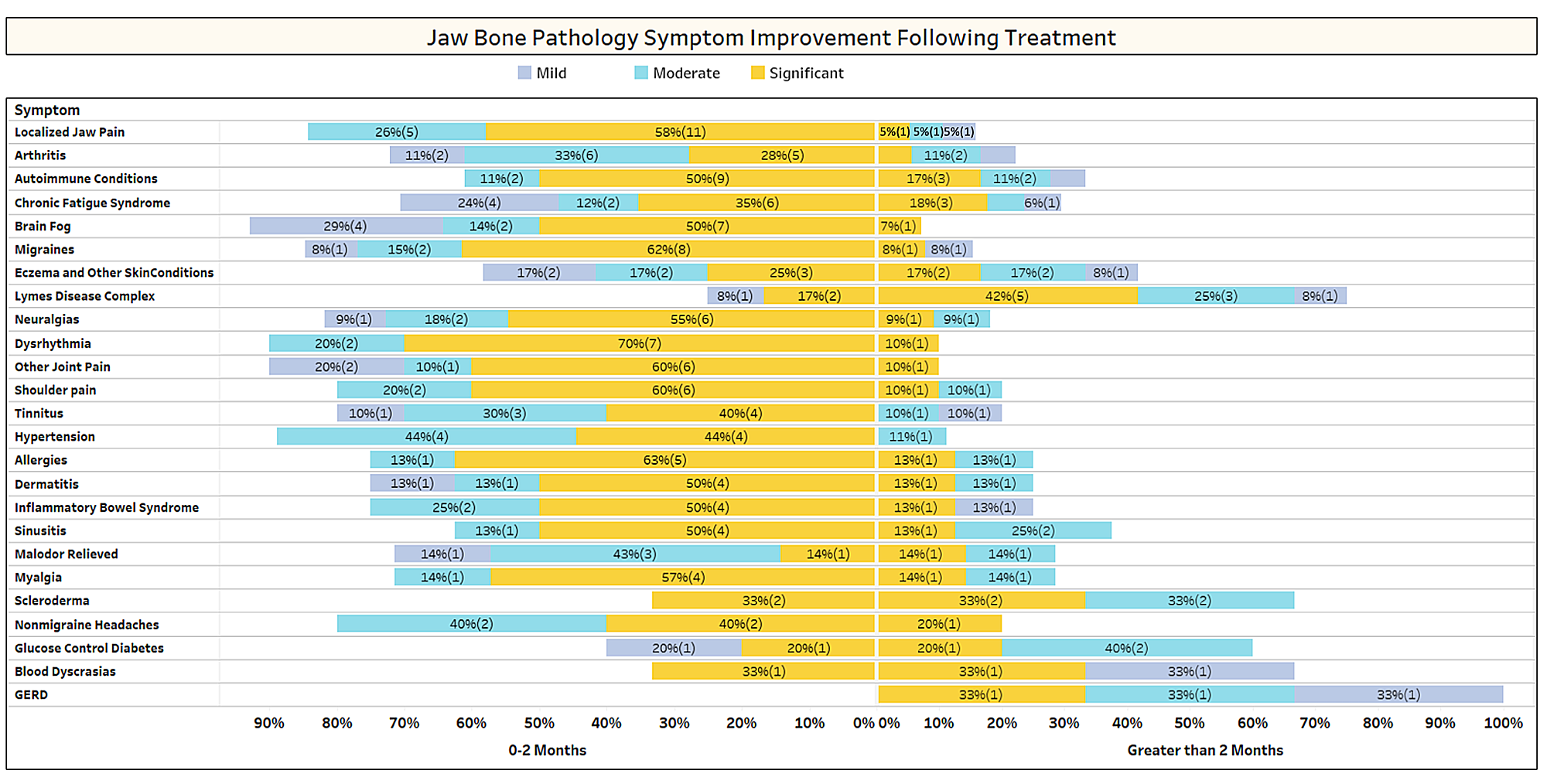
Anhang I Abb. 1 Die Befragten bewerteten den Grad der Verbesserung (leicht, mäßig oder erheblich) und gaben an, ob die Verbesserung schnell eintrat (0–2 Monate) oder länger dauerte (> 2 Monate). Die Erkrankungen/Symptome werden in der Reihenfolge aufgeführt, in der sie am häufigsten gemeldet werden. Beachten Sie, dass die meisten Beschwerden/Symptome in weniger als zwei Monaten zurückgingen (linke Seite der Mittellinie).
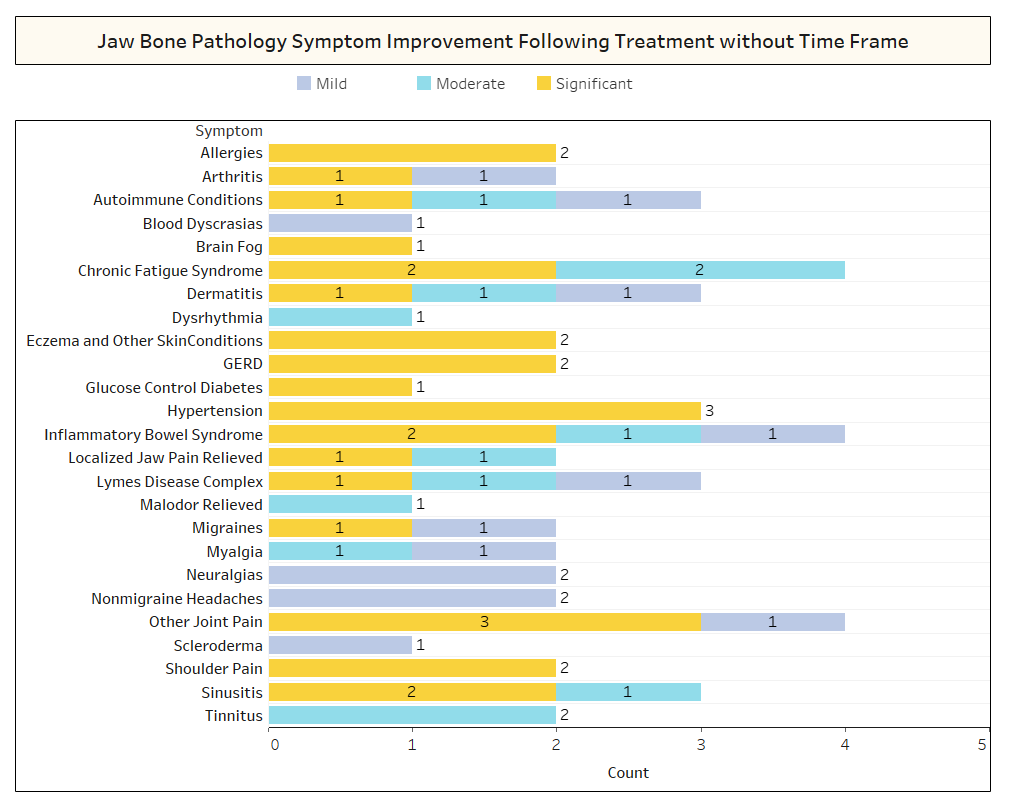
Anhang I Abb. 2 Wie oben gezeigt, haben die Befragten in mehreren Fällen den Zeitrahmen für die Wiederherstellung der beobachteten Verbesserungen nicht angegeben.
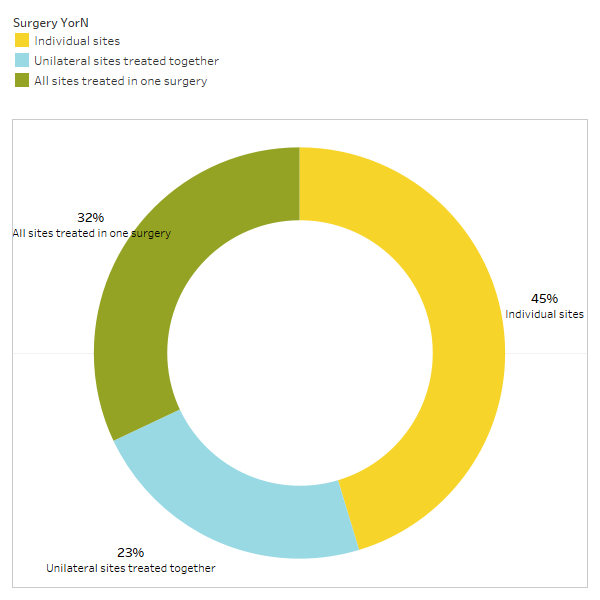
Anhang I Abb. 3 Die Befragten antworteten auf die Frage: „Empfehlen/erbringen Sie normalerweise?“
eine Operation für einzelne Stellen, einseitig behandelte Stellen zusammen oder alle Stellen, die in einer Operation behandelt werden?“
ERGEBNISSE DER IAOMT-UMFRAGE 1 (2021)
Aufgrund des Mangels an Literatur und klinischen Fallberichten zur Behandlung von Kavitationsläsionen befragte das IAOMT seine Mitglieder, um Informationen darüber zu sammeln, welche Trends und Behandlungen sich in Richtung eines „Versorgungsstandards“ entwickeln. Die vollständige Umfrage ist auf der IAOMT-Website verfügbar (beachten Sie, dass nicht alle Praktiker auf alle Umfragefragen geantwortet haben).
Um es kurz zusammenzufassen: Die Mehrheit der 79 Befragten bietet eine chirurgische Behandlung an, die eine Weichteilreflektion, einen chirurgischen Zugang zur Kavitationsstelle und verschiedene Methoden zur physischen „Reinigung“ und Desinfektion der betroffenen Stelle umfasst. Um die Heilung der Läsion vor dem Schließen des Weichteilschnitts zu fördern, wird eine breite Palette von Medikamenten, Nutrazeutika und/oder Blutprodukten eingesetzt.
Rotationsbohrer werden häufig verwendet, um die knöcherne Läsion zu öffnen oder Zugang dazu zu erhalten. Die meisten Ärzte verwenden ein Handinstrument zum Kürettieren oder Ausschaben des erkrankten Knochens (68 %), es kommen aber auch andere Techniken und Werkzeuge zum Einsatz, wie zum Beispiel ein Rotationsbohrer (40 %), ein piezoelektrisches Instrument (Ultraschall) (35 %) oder ein anderes Instrument ER:YAG-Laser (36 %), eine Laserfrequenz, die für photoakustisches Streaming verwendet wird.
Sobald die Stelle gereinigt, debridiert und/oder kürettiert ist, verwenden die meisten Befragten Ozonwasser/-gas zur Desinfektion und Förderung der Heilung. 86 % der Befragten nutzen PRF (Plättchenreiches Fibrin), PRP (Plättchenreiches Plasma) oder ozonisiertes PRF bzw. PRP. Eine vielversprechende Desinfektionstechnik, über die in der Literatur und in dieser Umfrage (42 %) berichtet wird, ist der intraoperative Einsatz von Er:YAG. 32 % der Befragten verwenden kein Knochentransplantat, um die Kavitationsstelle aufzufüllen.
Die meisten Befragten (59 %) führen in der Regel keine Biopsie der Läsionen durch und geben dafür verschiedene Gründe an: Kosten, die Unfähigkeit, lebensfähige Gewebeproben zu erhalten, Schwierigkeiten bei der Suche nach einem Pathologielabor oder Gewissheit über den Krankheitsstatus.
Die meisten Befragten verwenden keine Antibiotika präoperativ (79 %), während der Operation (95 %) oder postoperativ (69 %). Zu den weiteren verwendeten intravenösen Hilfsmitteln gehören Dexamethason-Steroide (8 %) und Vitamin C (48 %). Viele Befragte (52 %) nutzen postoperativ die Low-Level-Lasertherapie (LLLT) zu Heilungszwecken. Viele Befragte empfehlen eine Nährstoffunterstützung einschließlich Vitaminen, Mineralien und verschiedenen Homöopathika vor (81 %) und während (93 %) der Heilungsphase.
 Bilder
Bilder
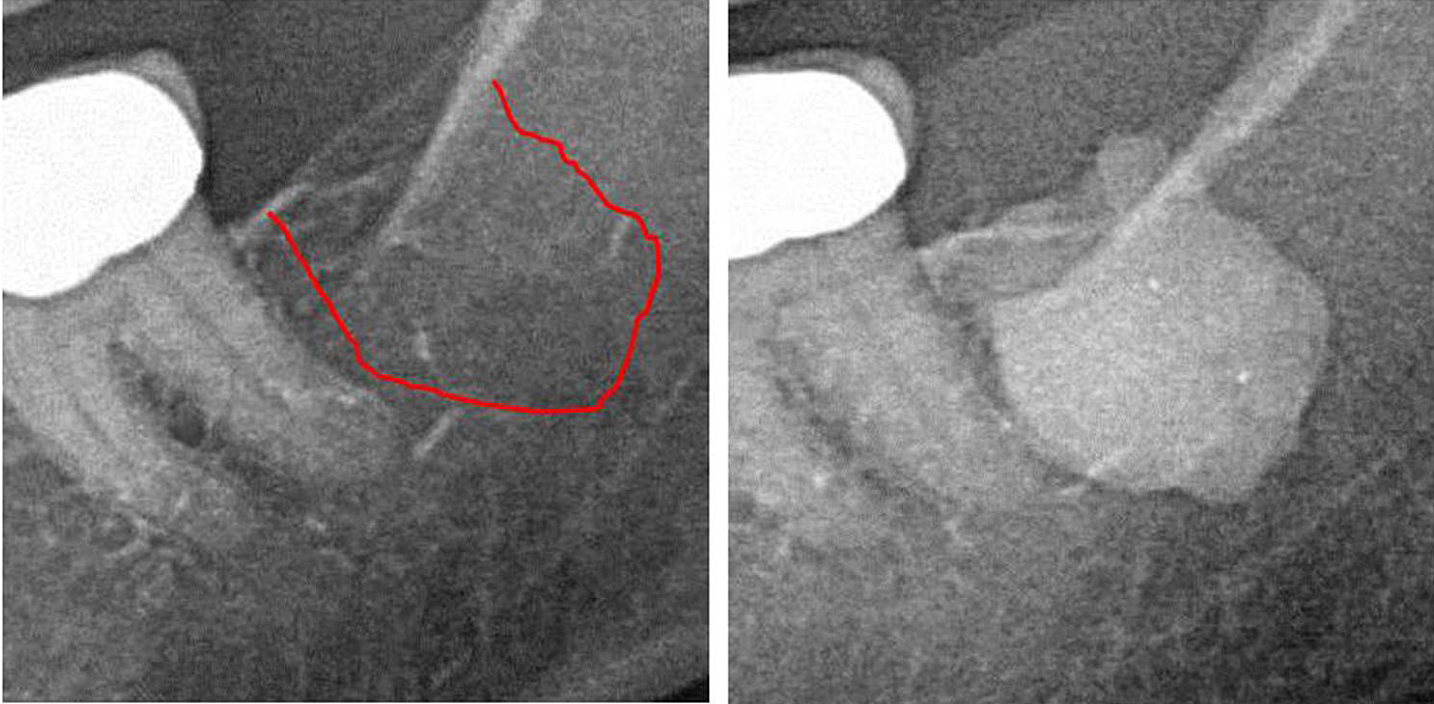
Anhang III Abb. 1 Linkes Feld: 2D-Röntgendiagnostik von Bereich Nr. 38. Rechtes Bild: Dokumentation der Ausdehnung des FDO im retromolaren Bereich 38/39 unter Verwendung eines Kontrastmittels nach der FDOJ-Operation.
Abkürzungen: FDOJ, fettige degenerative Osteonekrose des Kieferknochens.
Angepasst von Lechner et al., 2021. „Kieferknochenkavitation ausgedrückt RANTES/CCL5: Fallstudien, die eine stille Entzündung im Kieferknochen mit der Epistemologie von Brustkrebs verbinden.“ Brustkrebs: Ziele und Therapie
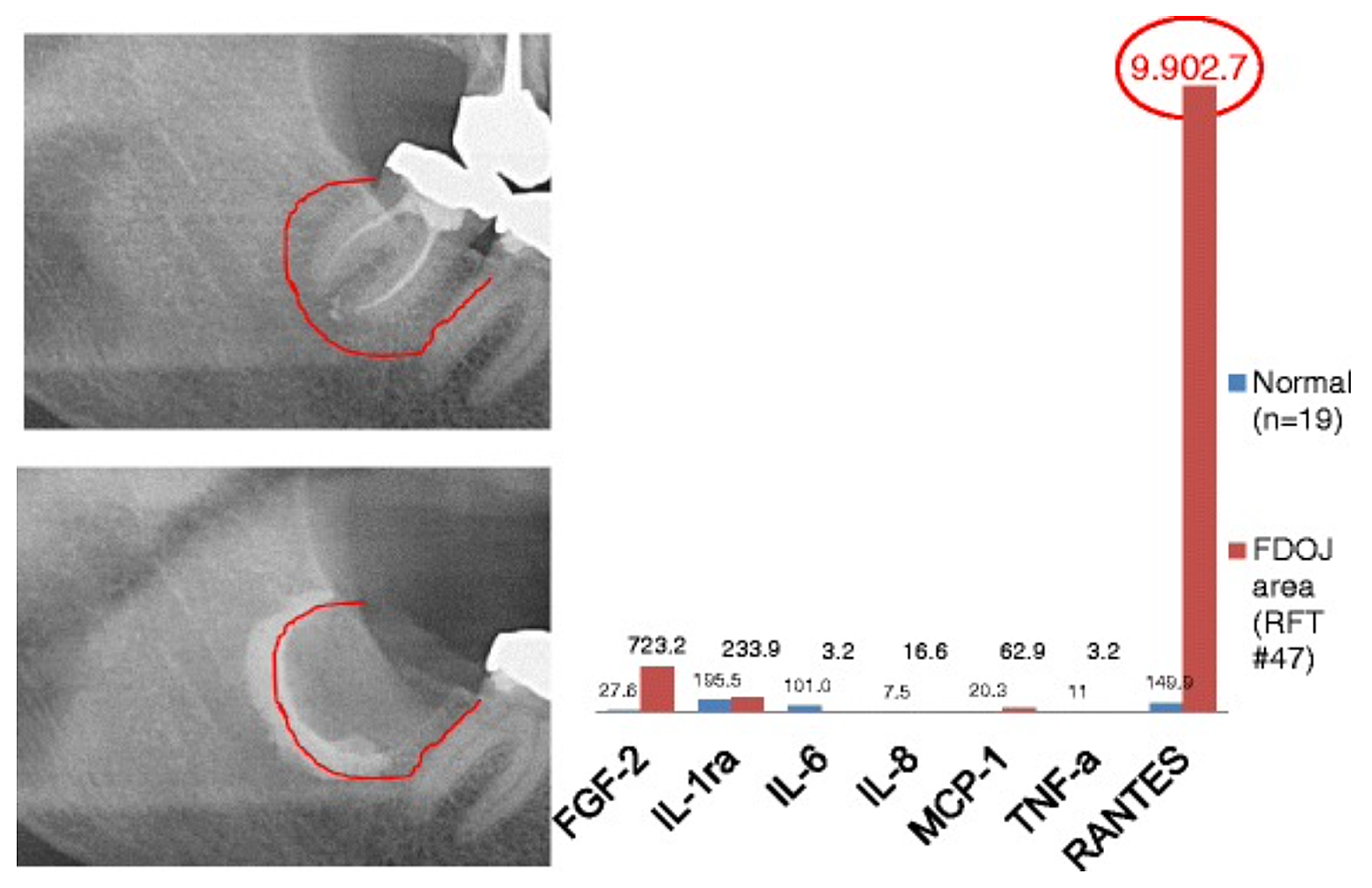
Anhang 3 Abb. 2 Vergleich von sieben Zytokinen (FGF-2, IL-1ra, IL-6, IL-8, MCP-1, TNF-a und RANTES) in FDOJ unter RFT #47 mit den Zytokinen im gesunden Kieferknochen (n = 19). Intraoperative Dokumentation der Ausdehnung des FDOJ im rechten Unterkieferknochen, Bereich Nr. 47 apikal von RFT Nr. 47, durch Kontrastmittel nach der chirurgischen Entfernung von RFT Nr. 47.
Abkürzungen: FDOJ, fettige degenerative Osteonekrose des Kieferknochens.
In Anlehnung an Lechner und von Baehr, 2015. „Chemokin RANTES/CCL5 als unbekannter Zusammenhang zwischen Wundheilung im Kieferknochen und systemischen Erkrankungen: Sind Vorhersagen und maßgeschneiderte Behandlungen in Sicht?“ Das EPMA-Journal
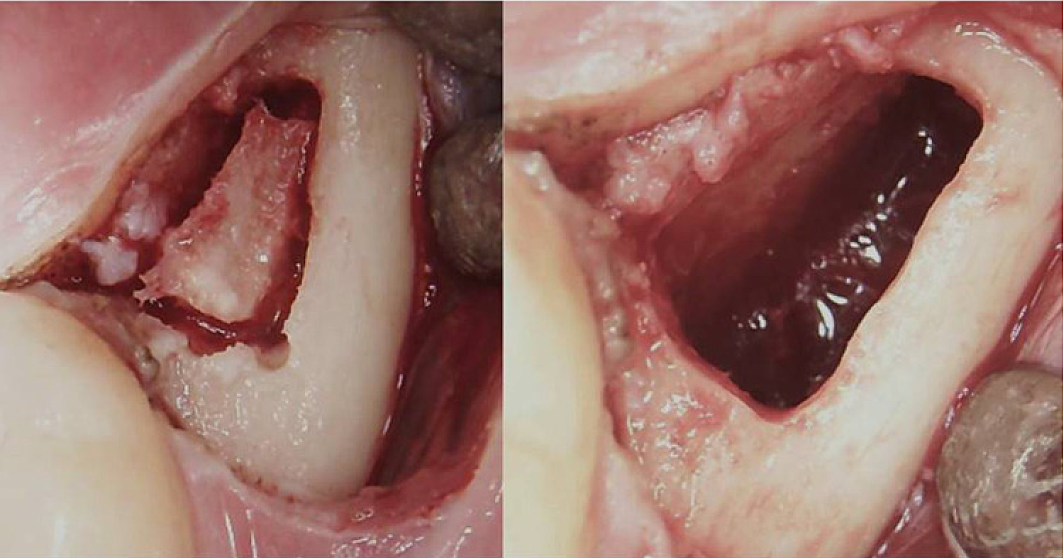
Anhang III Abb. 3 Chirurgischer Eingriff bei einem retromolaren BMDJ/FDOJ. Linkes Bild: Nach dem Herunterklappen des Mukoperiostlappens bildete sich in der Kortikalis ein Knochenfenster. Rechtes Bild: kürettierte Markhöhle.
Abkürzungen: BMDJ, Knochenmarkdefekt im Kieferknochen; FDOJ, fettige degenerative Osteonekrose des Kieferknochens.
Angepasst von Lechner, et al, 2021. „Chronisches Erschöpfungssyndrom und Knochenmarksdefekte des Kiefers – Ein Fallbericht zur zusätzlichen zahnärztlichen Röntgendiagnostik mit Ultraschall.“ Internationales Journal für medizinische Fallberichte
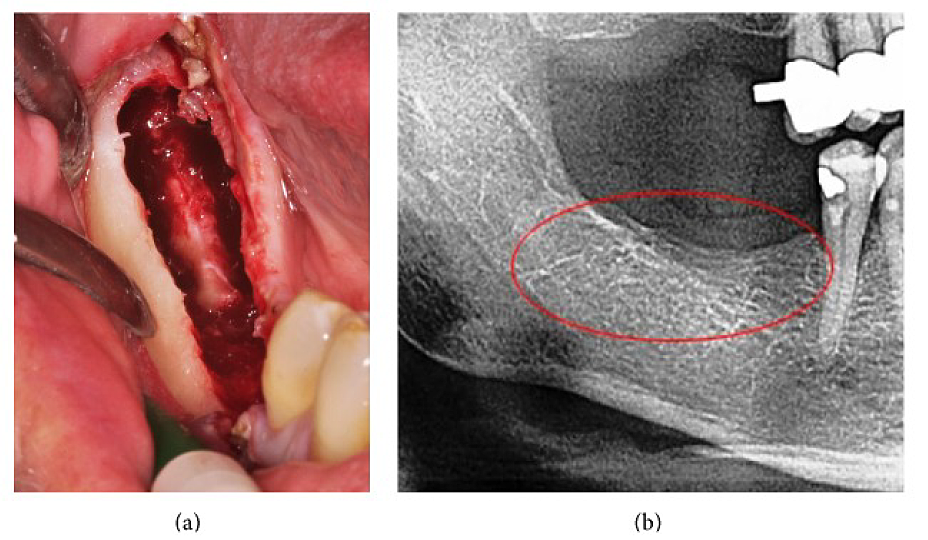
Anhang III Abb. 4 (a) Kürettage des FDOJ im Unterkiefer mit freigelegtem Nervus infraalveolaris. (b) Entsprechendes Röntgenbild ohne Anzeichen eines pathologischen Prozesses im Kieferknochen.
Abkürzungen: FDOJ, fettige degenerative Osteonekrose des Kieferknochens
Angepasst von Lechner et al., 2015. „Peripheral Neuropathic Facial/Trigeminal Pain and RANTES/CCL5 in Jawbone Cavitation.“ Evidenzbasierte Komplementär- und Alternativmedizin
Anhang III Film 1
Videoclip (doppelklicken Sie auf das Bild, um den Clip anzuzeigen) einer Kieferknochenoperation, die Fettkügelchen und eitrigen Ausfluss aus dem Kieferknochen eines Patienten zeigt, bei dem der Verdacht auf Kieferknochennekrose bestand. Mit freundlicher Genehmigung von Dr. Miguel Stanley, DDS
Anhang III Film 2
Videoclip (doppelklicken Sie auf das Bild, um den Clip anzuzeigen) einer Kieferknochenoperation, die Fettkügelchen und eitrigen Ausfluss aus dem Kieferknochen eines Patienten zeigt, bei dem der Verdacht auf Kieferknochennekrose bestand. Mit freundlicher Genehmigung von Dr. Miguel Stanley, DDS
Um diese Seite in einer anderen Sprache herunterzuladen oder auszudrucken, wählen Sie zunächst Ihre Sprache aus dem Dropdown-Menü oben links aus.
Autoren des IAOMT-Positionspapiers zu Kavitation im menschlichen Kieferknochen













